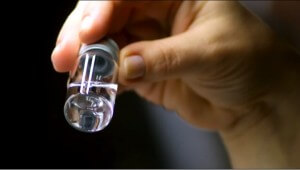
Si bien el objetivo principal de este capítulo es el control de partículas >50 micras, también comprende indicaciones sobre otros defectos como grietas en recipientes primarios o tapones mal ajustados.
La USP hace una declaración general sobre los posibles riesgos para el paciente debidos a la presencia de partículas en un inyectable, y los relaciona con el tamaño y el tipo de partículas presentes, y la edad o la condición del paciente.
Es interesante que durante el ciclo de vida de la inspección tiene en cuenta las posibles fuentes de partículas (tapón, vidrio, silicio, etc.) y solicita que se tomen las medidas necesarias para impedir cualquier generación de esas partículas.
También habla de evitar las partículas intrínsecas en el desarrollo mismo de los productos (prevención de la deslaminación del vidrio, elección de formulaciones apropiadas, estudios de estabilidad), y de la eliminación de partículas, por ejemplo, lavando recipientes primarios y realizando los estudios de eliminación de partículas asociadas
Como ya se ha descrito en el capítulo <790>, el AQL es parte de la evaluación de un lote, por lo que las muestras deben extraerse siguiendo planes de muestreo previamente definidos, y debe evaluarse la calidad del control 100% realizado. En el capítulo <17990> se dan ejemplos de los límites aceptables.
Se incorporan algunos consejos prácticos como mejorar la iluminación a 10.000 lux, y algunas formas de inspeccionar contenedores de plástico o de vidrio marrón, ya que la inspección visual de estos envases es difícil de realizar.
La cualificación y validación del proceso de inspección se refiere principalmente a la inspección visual manual. Se dan una serie de consejos para la creación de sets de patrones y para la cualificación y re-cualificación del personal. También se menciona el uso de Knapp tests para determinar las tasas de detección. Hay pocos consejos para la inspección automática y no se dice nada sobre la cualificación o re-cualificación de procesos de inspección totalmente automatizados.
El borrador del nuevo capítulo <1790> está disponible en la web de la USP.
El 08 de Junio en Barcelona y el 09 de Junio en Madrid, organizaremos la 2ª edición actualizada del curso de formación especializada: Inspección de partículas visibles en suspensión.

Soy de Buenos Aires , Argentina y estaré en España a fines de Junio y Julio, y estoy interesada en cursos de formación , exposiciones u otros eventos de la industría farmacéutica o sus proveedores, agradecere toda información que puedan facilitarme.
Atentamente
necesitaría conocer donde puedo encontrar proveedores de las mesas «blanca-negra» para inspección de partículas visibles en ojo humano que aparecen en las farmacopeas.
Gracias de antemano.
Alguién me podría recomendar un laboratorio en España especializado en caracterización de partículas visibles? gracias.